《自然》:绝了绝了!癌细胞利用T细胞的胞啃作用,把自己的抗原给了CAR-T细胞,让CAR-T自相残杀丨科学大发现
癌细胞确实让我们深恶痛绝。不过可恨之人必有可怜之处,癌细胞的生活也并不容易,无时无刻不在面对免疫系统的围追堵截。
为了逃避免疫系统的追杀,癌细胞可谓使尽了浑身解数,或表达PD-L1等免疫抑制分子,或减少呈递抗原的MHC分子表达,把自己隐藏起来。
然而昨天这项研究恐怕又要刷新我们对癌细胞伪装能力的认识了。纪念斯隆凯特琳癌症中心的Mohamad Hamieh和Michel Sadelain等研究发现,面对来势汹汹的CAR-T治疗,癌细胞竟然能把自身的抗原转移到CAR-T细胞上,在逃避免疫治疗的同时让CAR-T细胞自相残杀。相关研究发表在Nature上[1]。

Michel Sadelain的研究团队
CAR-T治疗,通过在患者自身的T细胞上引入肿瘤特异性嵌合抗原受体,让T细胞能更好地识别杀伤肿瘤,在很多血液系统肿瘤中取得了很好的效果[2]。
不过CAR-T效果虽好,肿瘤复发的问题却也屡见不鲜。而这些复发的癌细胞上,原本被CAR-T靶向的抗原,要么完全消失,要么大幅减少,让肿瘤对CAR-T治疗产生了耐药性[3]。
其中,完全丢失主要是由肿瘤的各种基因突变造成的[4],但那些抗原靶点大幅下调,却没有完全消失的癌细胞,是怎么让抗原靶点下调的却一直不清楚。对此,研究人员展开了研究。
研究人员对急性淋巴细胞白血病(ALL)模型小鼠,给予了有限的,分别携带CD28(19-28ζ)或者4-1BB(19-BBζ)共刺激因子的CAR-T治疗,模拟了CAR-T治疗后的复发。
2周后,输入的CAR-T消耗殆尽后,研究人员发现接受19-BBζ治疗的小鼠中的癌细胞上,CD19的表达量,从原来的平均每个细胞表达11000个CD19,下降到了4500个/细胞。但接受19-28ζ治疗的小鼠中,癌细胞CD19表达量没有变化。
为了搞清这些少了的CD19去哪了,研究人员在体外把癌细胞和19-BBζ共培养。仅仅1小时后,癌细胞上的CD19就大幅下降了,不过癌细胞中CD19的mRNA水平却没有明显的变化,而在共培养的19-BBζ CAR-T细胞上却出现了大量的CD19。
莫非癌细胞表面的CD19跑到了CAR-T细胞上?
研究人员给癌细胞的CD19分子接上了个荧光标签,共培养后,19-BBζ细胞表面果然出现了带荧光标签的CD19。还真是癌细胞把自己的表面抗原转移给了CAR-T细胞!
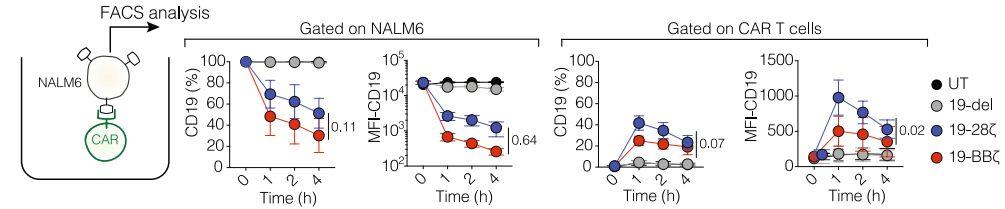
共培养下,癌细胞上CD19减少,而CAR-T上出现CD19
进一步研究发现,只有那些具有胞啃(trogocytosis,别笑,真这么翻译)能力的19-BBζ细胞,才会接受癌细胞上的靶抗原。
胞啃(实在忍不住就笑吧)是指淋巴细胞通过免疫突触,从抗原提呈细胞上啃下了一部分表面分子[5]。胞啃的功能目前还不是很清楚,可能对免疫反应的诱导和调节,以及其他细胞系统的控制有重要作用。不过在这里,胞啃成为了癌细胞对抗免疫治疗的利器。
除了减少癌细胞上的抗原数量,让癌细胞耐药外,胞啃还让CAR-T细胞带上了它所要攻击的靶点,使它们互相残杀。
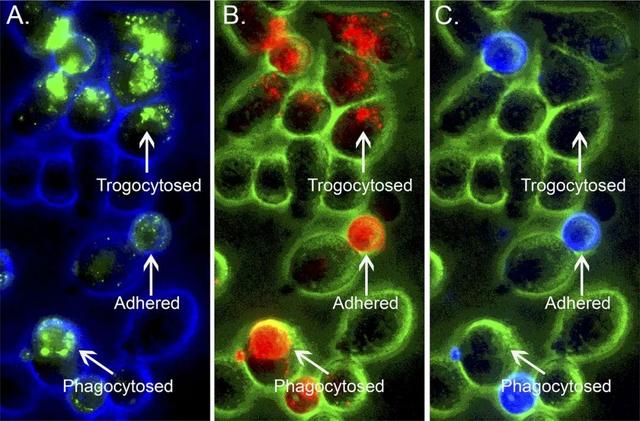
胞啃、粘附和吞噬
此外,治疗B细胞白血病的其它CAR-T靶点,如CD22、成熟B细胞抗原(BCMA)和间皮素(mesothelin)等,在相应的CAR-T治疗中,也出现了被靶向的癌细胞抗原转移到相应CAR-T细胞上的现象。
这一免疫治疗耐药机制或许普遍存在!
不过对于这种耐药,研究人员也给出了他们的解决方法——多靶点CAR-T治疗。在开始就联合使用19-BBζ和22-28ζCAR-T细胞,甚至让全部小鼠都活过了80天的试验期。
这么狡猾的癌细胞,还是被降服了。
编辑神叨叨
多管齐下避免耐药性这事并不新鲜,艾滋病的鸡尾酒疗法、化疗中多药联用,都是这个原理~
更多医学新进展尽在瞬息:
参考文献:
1. HAMIEH M, DOBRIN A, CABRIOLU A, et al. CAR T cell trogocytosis and cooperative killing regulate tumour antigen escape[J]. Nature, 2019.
2. Brudno J N, Kochenderfer J N. Chimeric antigen receptor T-cell therapies for lymphoma[J]. Nature reviews Clinical oncology, 2018, 15(1): 31.
3. Majzner R G, Mackall C L. Tumor antigen escape from CAR T-cell therapy[J]. Cancer discovery, 2018, 8(10): 1219-1226.
4. Orlando E J, Han X, Tribouley C, et al. Genetic mechanisms of target antigen loss in CAR19 therapy of acute lymphoblastic leukemia[J]. Nature medicine, 2018, 24(10): 1504.
5. Joly E, Hudrisier D. What is trogocytosis and what is its purpose?[J]. Nature immunology, 2003, 4(9): 815.



